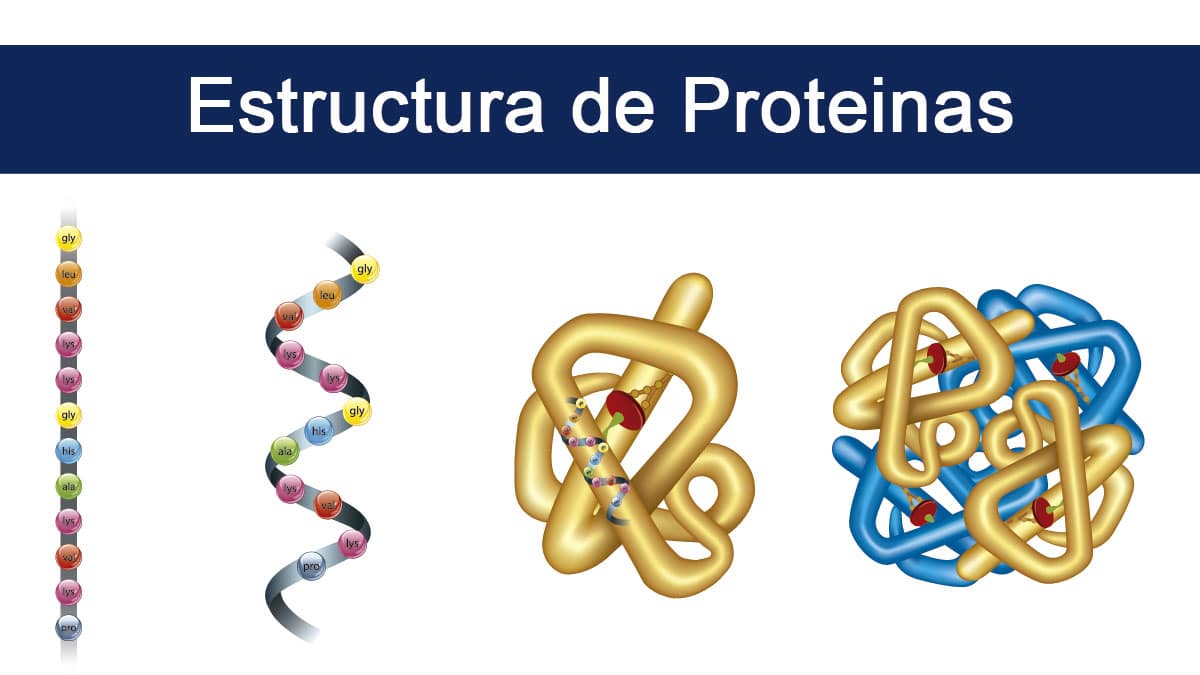
Un nuevo estudio realizado por químicos de la universidad de Arkansas muestra que el cristalograma de rayos x, el método estándar para determinar la estructura de las proteínas, puede proporcionar información inexacta sobre un conjunto crítico de proteínas los encontrados en las membranas celulares que a su vez podría estar llevando a un diseño de medicamentos pobre e insuficiente.
Los hallazgos del investigador fueron publicados hoy en informes científicos, una publicación de Nature.
Dos tercios de todas los medicamentos, incluyendo aquellas que son usadas por quimioterapia, la proteína que se encuentra en las membranas celulares, dijo Mahmoud Moradi, profesor asistente de química y bioquímica en el J. William Fullbright Colegio de arte y ciencias.
Desafortunadamente, el cristalograma de rayos X, el patrón oro para determinar la estructura de las proteínas, tiene muchas limitaciones cuando se trata de los que se encuentran en la membrana celular. Nuestro trabajo de exponer, y de muchas maneras, explica estas limitaciones.
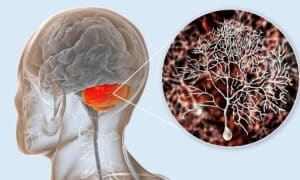
Considerado el trabajo de casa de las células, las proteínas son las responsables de casi toda una tarea en sistema viviente. Muchas proteínas viven dentro de la célula, y muchas residen en la membrana celular, una capa externa de lípidos que separa a la célula de su entorno externo.
La membrana proteica es importante porque regula el cambio de información y material entre la célula y su entorno, una tarea vital para la supervivencia y la función normal de la célula porque cualquier desorden en la función de la proteína puede ser resultado de una enfermedad.
El estudio de la función de la proteína es necesario para entender la base molecular de la enfermedad. Para hacer esto, investigadores han basado en la cristalograma de rayos X, la primera herramienta para determinar la forma y estructura de la proteína.
El cristalograma es además esencial para el diseño de fármacos que manipulan eficientemente la función de las proteínas. No obstante, el estudio de la estructura de la proteína de membrana es difícil porque su entorno natural no es compatible con la cristalograma de rayos X. Los investigadores deben quitar la proteína desde su entorno natural y colocarlos en un ambiente de lípidos artificiales antes de aplicar la técnica.
Moradi y Thomas Harkey -un estudiante universitario en ese momento y ahora un estudiante de medicina de la Universidad de Arkansas de Ciencias Medicina- añadió este problema desde un ángulo diferente. Aproximadamente hace dos años, usaron un superordenador en el centro de computación de alto rendimiento de Arkansas funcionará de manera continua, cálculos de microsegundo nivel que simulan la dinámica molecular de YidC2, una membrana de proteína con una ansa citoplasmática sin resolver cristalográficamente en su estructura molecular. Se sabe que los lazos citoplasmáticos tienen importancia funcional en las proteínas de la membrana.
Las simulaciones de Moradi y Harkey demostraron que el ansa citoplasmática de YidC2 estabilizaba toda la proteína, en particular la región c1, un área potencialmente importante para el diseño de fármacos. Este hallazgo demostró que los bucles no resueltos de proteínas de membrana podrían ser importantes para la estabilización de las proteínas, a pesar de la aparente falta de estructura molecular.
Típicamente, si parte de la proteína no es resuelta en cristalografía de rayos x, es interpretado como carece de una estructura particular, dijo Moradi. Mostramos que por la membrana de proteína y en particular partes de la proteína que interacciona con la membrana celular, esta interpretación no es exacta y puede ser engañosa.
Pensamos que la explicación alternativa para la enfermedad puede ser que la proteína no es estudiada en su membrana natural. Moradi dijo que su resultado además de demostrar que la química computacional y la supercomputación tecnológica pueden ser usados como prototipo la membrana de proteína es mayor precisión en un entorno que los imitadores en su entorno psicológico.